新闻中心
NEWS
基于DNA参考物质的BRAF V600E突变数字PCR定量检测室间评比
微滴式数字PCR(Droplet digital PCR, ddPCR)因其超高的灵敏度,可检测病人血液中与肿瘤相关的痕量循环肿瘤DNA(Circulating tumor DNA, ctDNA)标志物而获得多方瞩目。在全球范围内,众多医学检验所已可提供各种基于ddPCR的自建临床检测服务,而ddPCR要正式进入IVD应用,用于性能验证和评估的通用标准参考物质显得尤为重要。
国家计量研究院、南京测量与测试技术研究所、北京理化分析中心等多家单位设计、推出了可国际单位量值溯源 的BRAF V600E ctDNA标准参考物质(SI-traceable RM),并使用该标准物质开展了国内8家实验室的室间评比,以测试不同实验室对低水平BRAF 突变的定量检测能力。
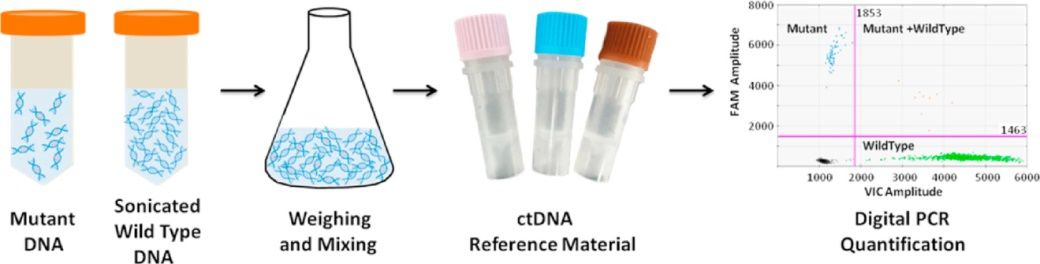
如Fig. 1 所示方案,计量研究院的专家们分别制备并定量了纯化的含突变型DNA的152bp PCR扩增产物和经超声波片段化的野生型gDNA,以模拟ctDNA的状态;将PCR产物和野生型gDNA按照重量比例混合以制备不同突变丰度梯度。总共制备高中低3个不同突变丰度的标准物质,最终拷贝数浓度和突变丰度通过重量法和ddPCR进行表征。

Fig. 1 . ctDNA标准参考物质的制备方案及流程
标准物质的ddPCR分析标定在Bio-Rad QX200 ddPCR上进行,并按照EP17-2指南测定了QX200的动态范围、LoB、LoD和LoQ(Fig. 2)。在突变丰度53.9%~0.1%范围内,QX200定量结果和理论值一致性良好, LoB、LoD和LoQ分别为0.01%、0.02%和0.1%。

Fig. 2 标准物质在QX200 ddPCR上的检测效果。
A. BRAF V600E ddPCR MGB assay的二维散点图;B. NTC 对照的二维散点图(无污染发生)
专家们还测试了QX200 ddPCR和NGS(illumina NextSeq 500)数据一致性,在0.54%~43.98%突变丰度范围内,QX200 ddPCR和NGS结果相关系数达0.92,确认了QX200 ddPCR突变丰度数据的可靠性。值得注意的是本测试中,NGS不能检出突变丰度在0.3%的样本,QX200 ddPCR的灵敏度要高于NGS(Table 1)。
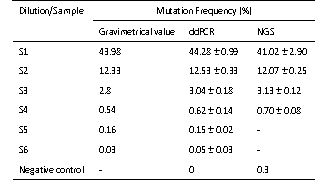
Table 1 QX200 ddPCR和NGS对BRAF V600E标准物质突变丰度的检测比较
参照ISO5715-1,不同浓度的标准参考物质被发送给8家实验室,各自分别检测BRAF V600E突变丰度以及突变型、野生型的绝对拷贝数浓度,以评测ddPCR的室间重复性和重现性。其中七家实验室(Lab 1-3, 5-8)使用Bio-Rad QX200 ddPCR系统,一家(Lab 4)使用了Stilla Naica Crystal ddPCR平台。每个浓度水平的标准物质均设置5个技术重复,所有原始数据均提交给国家计量院并采用自动分析模式进行数据处理。
各参比实验室的数据显示ddPCR能准确检测低水平的突变丰度,但Naica Crystal ddPCR平台存在系统偏差,对野生型和突变型靶标的绝对定量数值与其他实验室的结果有显著差异,并且与计量院标准物质的赋值也有显著差异(Fig. 3)。在修正了微滴体积之后,Naica crystal ddPCR的定量结果准确性有了提升,这凸显了微滴体积的偏差(实际微滴体积和软件中用以计算结果的默认微滴体积之间的差异)对ddPCR定量结果准确性的影响。
国家计量院等单位的这项研究有重要意义:
一方面提出并验证了一个突变标准参考物质的制备和标定方法,提示ddPCR的计量学价值;
另一方面使用标准物质开展了ddPCR室间评比,不仅评估了ddPCR的重复性、再现性,还解决了准确性评估的问题,为ddPCR检测方法,特别是实验室自建检测(LDT)方法的验证和确认,以及医学检验室检测能力的建设和提高提供了技术手段。
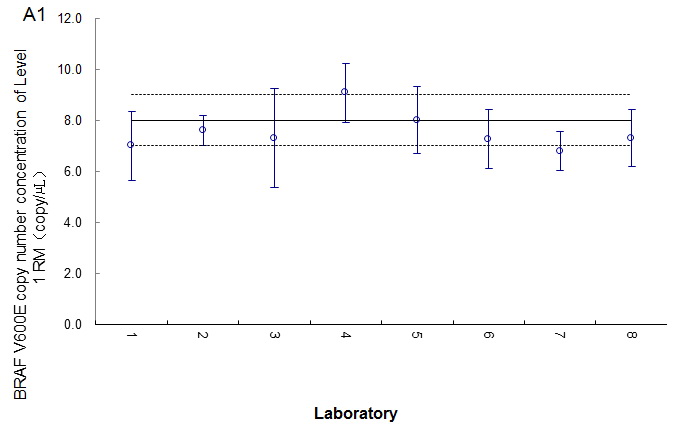
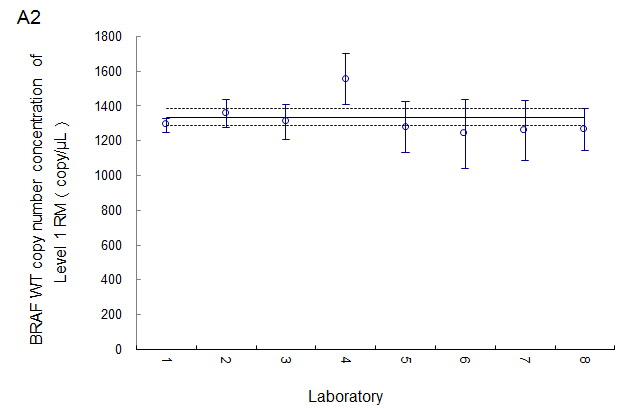

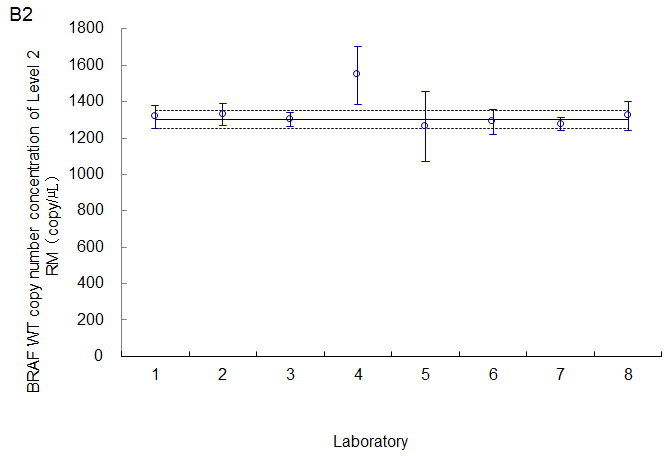


Fig. 3突变拷贝数(A1, B1, C1)和野生型拷贝数(A2, B2, C2) 的室间评比数据。
8家实验室测试了3个不同突变水平的BRAF V600E标准物质不中突变序列和野生型序列的拷贝数。4为使用Naica Ctrystal ddPCR的实验室数据。实线为平均ddPCR和重量分析法数据的标准物质特性值,虚线为特性值均数的拓展不确定度(95%CI)。

电话:021-61283010
网址:www.bio-chain.com
邮箱:marketing@bio-chain.com
地址:上海市徐汇区虹漕路421号65幢303室
上海柏辰生物科技有限公司 版权所有 严禁复制 网站备案号:沪ICP备09099502号-1 沪公网安备 31010402002899号 网站建设:铭心科技



